ЛАБОРАТОРНА РОБОТА 2
ТЕМА «Визначення йона феруму (ІІІ) у питній воді»
Мета - оволодіти прийомами фотометричного визначення йона феруму (ІІІ) у питній воді
Теоретичні відомості
Визначення йона феруму (ІІІ) у питній воді базується на утворенні інтенсивно забарвленого розчину при взаємодії йона феруму (ІІІ) із сульфосаліциловою кислотою, інтенсивність забарвлення якого пропорційна вмісту йона ферума (ІІІ) у розчині.
Для вимірювання інтенсивності світла, яке проникло через забарвлену рідину, використовують фотоелектро- колориметри (ФЕК-М, ФЕК-56, КФК-2МП).
Експериментальна частина
Матеріали та реактиви: сульфосаліцилова кислота, 10% розчин; залізо-амонійний галун (стандартний розчин містить 0,1 мг йона феруму (ІІІ) в 1 мл); сульфатна кислота, 0,5 М розчин; амоніак, 10% розчин; аналітичні терези; КФК-2МП; мірні колби місткістю 50 см3; піпетки.
Будова калібрувального графіка
Послідовно у 6 мірних колб вливають 0, 2, 4, 6, 8, 10 см3 стандартного розчину залізоамонійного галуну (стандартний розчин готують у мірній колбі місткістю 1000 см3: розчиняють 0,8636 г галуну в дистильованій воді, підкислюють сульфатною кислотою до рН 2, об’єм розчину доводять дистильованою водою до позначки). Додають у кожну колбу по 3 см3 розчину сульфосаліцилової кислоти, 1 см3 сульфатної кислоти і доводять до позначки дистильованою водою, перемішують. Одержують серію розчинів червоно-фіолетового кольору, які містять 0; 0,2; 0,4; 0,6; 0,8; 1,0 мг йона феруму (ІІІ) у 50 см3 розчину.
Оптичну густину виміряють як це описано в Лабораторнй роботі №1 при довжині падаючого світла 540 нм. Вимірювання проводять 3 рази. Дані заносять до таблиці 2.1. За отриманими даними будують градуювальний графік у координатах: оптична густина – вміст йона феруму (ІІІ), мг/50 см3.
Таблиця 2.1
|
Вміст Fe3+, мг/50 см3 |
0 |
0,2 |
0,4 |
0,6 |
0,8 |
1,0 |
Досл. |
|
Оптична густина D |
|||||||
|
Оптична густина Dсер |
Побудова калібрувального графіка і визначення концентрації речовини в дослідній воді.
|
D
С Fe+3 (мг/50мл) |
Рис 2.1. Калібрувальний графік для визначення вмісту Феруму в дослідній воді.
Хід визначення.
У мірну колбу місткістю 50 см3 вливають 25 см3 дослідної води (видається викладачем), додають 3 см3 розчину сульфосаліцилової кислоти, 1 см3 сульфатної кислоти і об’єм доводять до позначки дистильованою водою, перемішують.
Одержують приготовлений контрольний розчин у викладача з невідомим вмістом іонів заліза .Вимірюють оптичну густину (як зазначено вище) не менше 3 разів, кожний раз наливають новий розчин у кювету. Розраховують середню величину густини і визначають вміст йона феруму (ІІІ) за калібрувальним графіком у 50 см3 розчину. Для цього відміряють величину D на осі ординат і проводять до неї перпендикуляр до перетину прямої, опускають перпендикуляр на вісь абсцис і визначають концентрацію.
Для більш точного визначення в програмі Excel побудувати графік залежності оптичної густини від вмісту іонів феруму D (CFe), використовуючи значення з таблиці 2.1, та визначають рівняння лінії тренда. За рівнянням визначають вміст іонів заліза в дослідній воді (контрольний розчин)
Вміст йона феруму (ІІІ) в 1 дм3 дослідної води (мг/см3) розраховують за рівнянням
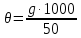
де g ─ вміст йона феруму (ІІІ) в 50 см3 дослідної води за калібрувальним графіком.
Роблять висновок, у якому порівнюють значення вмісту йонів феруму (ІІІ) з санітарними нормами, та роблять висновок про можливість застосування води для вживання та застосування у різних технологічних процесах.
Запитання для самоперевірки
-
-
Фізико-хімічні методи аналізу, їх перевага та взаємозв’язок із хімічними методами аналізу.
-
Сформулюйте закон Бугера-Ламберта-Бера і запишіть для нього математичний вираз.
-
Теоретичні основи колориметрії.
-
Яка фізична суть молярного коефіцієнта поглинання? Від яких чинників він залежить?
-
Що таке оптична густина розчину? Як вона залежить від концентрації речовини та товщини шару розчину?
-
Наслідки основного закону колориметрії.
-
Як класифікуються колориметричні методи аналізу? Суть методу.
-
Практичне застосування колориметричного аналізу.
-
При проникненні світла через шар розчину товщиною 1 см інтенсивність його зменшилась на 10 %. Яка буде інтенсивність світла, що проникло через шар цього ж розчину товщиною 10 см?
-





