- 2.1 Человеческое общество и проблема энергии
- 2.2 Использование энергии в химической промышленности
- 2.3 Источники энергии
- 2.4 Рациональное использование энергии в химической промышленности
- 2.5 Новые виды энергии в химической промышленности
Ключові терміни:
вторичные энергоресурсы, калорийный эквивалент, количество энергии, теплоноситель, энергоемкость производства2.1 Человеческое общество и проблема энергии
Одним из условий существования человеческого общества является непрерывный обмен энергией с окружающей средой. Поэтому энерговооруженность общества составляет условие прогресса человечества, а дальнейшее развитие материальной культуры непосредственно связано с решением энергетической проблемы. Уровень материального благосостояния современного общества определяется количеством энергии, вырабатываемой на душу населения.
Потребление энергии на планете непрерывно возрастает. Если в 1975 году оно составляло 0,25Q, то прогноз на 2000 год дает 0,8Q, а на 2100 год астрономическую цифру 7,3Q, где Q=2,3×1014 кВт×ч. Производство энергии в РФ в 1992 году было эквивалентно 1,6 т условного топлива на человека.
Предполагается, что в 2100 году оно достигнет 1,8-2,0 т УТ. Структура потребления энергии в современном обществе свидетельствует, что наиболее энерговооруженной отраслью народного хозяйства является промышленное производство, а наименее – сельское хозяйство.
Существует определенная связь между потреблением энергии обществом и средней продолжительностью человеческой жизни, как это видно из рис. 2.1.
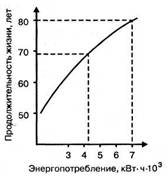
Рисунок 2.1 – Зависимость продолжительности челове-ческой жизни от величины энергопотребления
Из него следует, что «порог» энергопотребления, при котором достигается устойчивая средняя продолжительность жизни порядка 80 лет, равен 7×103 кВт×ч на человека в год. Этот порог достигли, или приблизились к нему такие страны как Швеция, ФРГ, США, Япония.
2.2 Использование энергии в химической промышленности
Химическое производство принадлежит к числу наиболее энергоемких. Так, если в продукции всей промышленности доля затрат на энергию составляет 2,5%, то в продукции нефтехимической и химической отраслей она достигает 8,9%. Химическая отрасль промышленности, производя около 6% промышленной продукции, потребляет до 12% всей вырабатываемой электроэнергии. Эта высокая энергоемкость обусловлена значительным потреблением энергии такими химическими производствами, как производство аммиака, фосфора, карбида кальция, карбоната натрия, химических волокон и пластмасс, которое составляет более 60% электрической и 50% тепловой энергии всей отрасли.
Потребление энергии химическим производством оценивается его энергоемкостью. Энергоемкость производства - количество энергии, затрачиваемое на получение единицы продукции. Она выражается в кВт-ч (кДж) или в тоннах условного топлива (УТ) на тонну продукции. По энергоемкости химические производства делятся на три класса.
І-ый класс. Производства с расходом УТ более 2 тонн (58×103кДж) на тонну продукции. К ним относятся производства химических волокон, ацетилена, капролактама, полиэтилена, акрилонитрила и др.
ІІ-ой класс. Производства с расходом УТ от 1 до 2тонн (29×103 - 58×103 кДж) на тонну продукции. К ним относятся производства карбоната натрия, аммиака, карбида кальция, метанола и др.
III-ий класс. Производства с расходом УТ менее 1тонны (29×103 кДж) на тонну продукции. К ним относятся производства разбавленной азотной кислоты, этиленгликоля, уксусной кислоты, анилина, полистирола, двойного суперфосфата и др.
Энергоемкость отдельных производств колеблется в очень широких пределах: от 20×103 кВт×ч для алюминия до 60-100 кВт×ч для серной кислоты на тонну продукции.
В химическом производстве энергия используется для проведения химических реакций, сжатия газов и жидкостей, нагрева материалов, осуществления тепловых процессов (ректификация, испарение и др.), проведения механических и гидродинамических процессов (измельчение, фильтрование идр.), транспортировки материалов. Для этих целей используется электрическая, тепловая, топливная, механическая, световая, ядерная и химическая энергия.
Электрическая энергия применяется для проведения электрохимических, электротермических, электромагнитных и электростатических процессов, а также для перемещения материалов и приведения в действие различных механизмов и машин.
Тепловая энергия используется для различных целей. Энергия высокого потенциала (более 623°К) применяется для высокотемпературной обработки сырья (обжиг и др.) и интенсификации химических реакций. Ее получают за счет сжигания различных видов топлива непосредственно в технологических устройствах. Тепловая энергия среднего (373-623°К) и низкого (323-423°К) потенциала используется в производственных процессах, связанных с изменением физических свойств материалов (нагрев, плавление, дистилляция, выпаривание), для нагрева компонентов при химических процессах, а также для проведения некоторых химических процессов.
Передача тепла осуществляется за счет контакта нагреваемой системы через стенку аппарата с теплоносителем, обладающим высоким теплосодержанием или при непосредственном контакте с нагреваемым материалом. Теплоноситель - вещество или система веществ, используемое в качестве среды для нагревания. В качестве теплоносителей для средне- и низкотемпературных процессов в химической промышленности применяются горячий воздух, горячая вода, насыщенный и перегретый водяной пар, топочные газы, высококипящие органические соединения, твердые зернистые материалы (обычно зерна катализатора).
Топливная энергия при сжигании топлива используется для производства тепла и электроэнергии в ТЭЦ и печах особого назначения и составляет в общем балансе энергии, используемой в химической промышленности, около 50%.
Механическая энергия используется для выполнения таких физических операций как измельчение, центрифугирование, перемещение материалов, смешение в работу различных машин, компрессоров, насосов и вентиляторов и др.
Световая энергия применяется в виде облучения для проведения фотохимических процессов синтеза, например, в производстве хлороводорода, галогеналканов и др.
Химическая энергия реализуется в работе химических источников тока различного устройства и назначения.
Ядерная энергия используется для проведения радиационно-химических процессов (например, в процессах полимеризации), производства энергии в АЭС, для анализа, контроля и регулирования процессов производства.
Из всей потребляемой химической промышленностью энергии 40% составляет электрическая, 50% - тепловая (в виде теплоносителей - пара и воды) и 10% топливная энергия.
2.3 Источники энергии
Основными источниками энергии, потребляемой промышленностью, являются горючие ископаемые и продукты их переработки, энергия воды, биомасса и ядерное топливо. В значительно меньшей степени используются энергия ветра, солнца, приливов, геотермальная энергия. Мировые запасы основных видов топлива оцениваются в 1,28×1013 тонн УТ, в том числе, ископаемые угли 1,12×1013тонн, нефть 7,4×1011 тонн и природный газ 6,3×1011тонн УТ.
Выработка энергии на планете в настоящее время составляет 2,93×1014 кВт×ч или 3,35×107 МВт×год.
Все энергетические ресурсы подразделяются на первичные и вторичные, возобновляемые и невозобновляемые, топливные и нетопливные (рис. 2.2).
Эксплуатация невозобновляемых энергоресурсов приводит и их исчерпанию и уменьшению энергетического потенциала планеты, а с другой стороны повышению температуры среды обитания. Поэтому они называются также «добавляющими» тепло источниками энергии. Эксплуатация возобновляемых энергоресурсов сохраняет энергетический потенциал планеты и не изменяет температуру среды обитания. Поэтому они называются «недобавляющими» тепло источниками энергии.
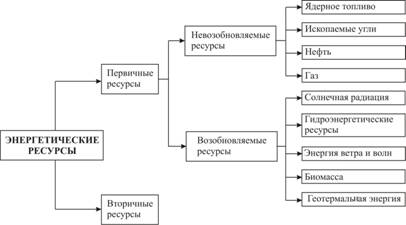
Рисунок 2.2 – Классификация энергетических ресурсов
К топливным энергетическим ресурсам относятся уголь, нефть, природный газ, сланцы, битуминозные пески, торф, биомасса. К нетопливным - гидроэнергия, энергия ветра, лучистая энергия Солнца, глубинная теплота Земли и др.
Вторичные энергоресурсы (ВЭР) - энергетический потенциал конечных, побочных и промежуточных продуктов и отходов химического производства, используемый для энергоснабжения агрегатов и установок. К ВЭР относятся тепловые эффекты экзотермических реакций, теплосодержание отходящих продуктов процесса, а также потенциальная энергия сжатых газов и жидкостей. Наибольшими ВЭР (главным образом в форме тепла) располагают предприятия химической, нефтеперерабатывающей и нефтехимической промышленности, металлургии, промышленности строительных материалов, газовой промышленности, тяжелого машиностроения и некоторых других отраслей народного хозяйства.
Важнейшим источником энергии является химическое топливо (ископаемые угли, торф, нефтепродукты, природные и технические газы), составляющие в балансе энергоресурсов химической промышленности до 70%. Структура потребления химического топлива такова: газ 19,4%, твердое топливо 30,9%, нефтепродукты 47,2%.
Энергетическая ценность химического топлива характеризуется калорийным эквивалентом и количеством энергии:
-
калорийный эквивалент ηк- отношение низшей теплоты сгорания данного топлива к теплоте сгорания УТ, принимаемой за 29260 кДж:
- [TEX]\eta к=\frac{Qк}{29260} [/TEX], (2.1)
- количество энергии в кВт•ч – энергия, получаемая при полном сгорании 1 кг или 1 нм3 топлива. Эта величина составляет: для каменного угля 8,0, природного газа 10,6, кокса 7,2, мазута 15,4, обратного коксового газа 4,8. Для сравнения та же величина для обогащенного урана равна 22,5×106.
Второе место по масштабам энергетического вклада занимают гидроэнергия (ГЭС) и ядерная энергия (АЭС). Доля энергии, вырабатываемой ГЭС составляет около 12%. Дальнейшее развитие гидроэнергетики связано с экологическими проблемами, к числу которых относится сокращение площади плодородных земель и изменение климата при строительстве равнинных ГЭС.
АЭС представляют наиболее перспективный источник энергии как электрической, так и тепловой.
Истощение энергоресурсов привело к необходимости изыскания новых видов и источников энергии. К ним относятся водород, а также возобновляемые источники энергии в виде гидроэнергии, энергии ветра и приливов, геотермальной энергии.
Использование водорода в качестве источника энергии определяется следующими его преимуществами как топлива:
- распространением водорода (в литосфере 17 атомов на 100 атомов) и практически неисчерпаемыми запасами воды как источника водорода;
- высоким энергосодержанием, превышающим в 3,5 раза энергосодержание нефти;
- простотой и дешевизной транспортировки (передача водорода дешевле передачи электроэнергии);
- экологической чистотой продуктов сгорания.
Производство водорода в промышленных масштабах с достаточной степенью экономичности может быть осуществлено электролизом воды, пиролизом воды в плазмотроне, обработкой биомассы водяным паром, фоторазложением воды в присутствии ферментов, проведением термохимических и термоэлектрохимических циклов разложения воды.
Термохимические циклы представляют собой чередование экзо- и эндотермических процессов и протекают при относительно низких температурах (схема «теплового насоса»):
- M +H2O = H2 + MO - ΔH,
- MO + M = 0.5O2 + 2M +ΔH.
Комбинированные термоэлектрохимические циклы осуществляются с использованием на одной из стадий энергии АЭС:
- M +H2O = H2 + MO - ΔH,
- 2MO → 2M 2M + O2 + ΔH ,
- где М - реагент с большим, чем у водорода сродством к кислороду, что обеспечивает термодинамическую возможность процесса при относительно низкой температуре;
- МО- оксид, легко диссоциирующий при нагревании.
Использование других альтернативных источников энергии ограничивается проблемой «концентрации энергии» (H.H. Семенов). Так, например, все энергетические потребности человечества может удовлетворить всего 0,5% солнечной энергии, падающей на землю. Однако для ее поглощения и утилизации необходимы гелиоустановки общей площадью 130000 км2. В связи с этим возникает задача изыскания более технологичных концентрированных видов энергии. Она может быть решена переходом от традиционной схемы выработки электрической энергии через механическую
к схеме непосредственного превращения тепловой энергии в электрическую
![]() .
.
Для этой цели используются:
- магнитогидродинамические генераторы (МГД-генераторы), в которых кинетическая энергия низкотемпературной плазмы за счет торможения в магнитном поле переходит в электрическую энергию постоянного тока;
- топливные элементы (электрохимические генераторы), в которых осуществляется непосредственное превращение энергии горения реакционноспособных топлив (водород, спирты, альдегиды и другие активные восстановители) в электрическую энергию.
В обоих случаях КПД этого процесса существенно превышает КПД традиционных процессов.
2.4 Рациональное использование энергии в химической промышленности
Высокая доля энергии в себестоимости химической продукции обусловила необходимость ее рационального и экономичного использования в производстве. Критерием экономичности использования энергии всех видов является коэффициент использования энергии, равный отношению количества энергии, теоретически необходимой на производство единицы продукции (WT), к количеству энергии, практически затраченной на это (Wп):
[TEX]\eta = \frac{Wт}{Wп} [/TEX]. (2.2)
Для высокотемпературных эндотермических процессов коэффициент использования тепловой энергии не превышает 0,7, то есть до 30% энергии уходит с продуктами реакции в виде тепловых потерь.
Рациональное использование энергии в химическом производстве означает применение методов, повышающих коэффициент использования энергии. Эти методы могут быть сведены к двум группам: разработке энергосберегающих технологий и улучшению использования энергии в производственных процессах. К первой группе методов относятся:
- разработка новых энергоэкономных технологических схем;
- повышение активности катализаторов;
- замена существующих методов разделения продуктов производства на менее энергоемкие (например, ректификации на экстракцию и т. п.);
- создание комбинированных энерготехнологических схем, объединяющих технологические операции, протекающие с выделением и поглощением энергии (теплоты). Подобное сочетание в одном производстве энергетики и технологии позволяет значительно полнее использовать энергию химических процессов, другие энергоресурсы и повысить производительность энерготехнологических агрегатов.
Ко второй группе энергосберегающих методов относятся:
- уменьшение тепловых потерь за счет эффективной теплоизоляции и уменьшения излучающей поверхности аппаратуры;
- снижение потерь на сопротивление в электрохимических производствах;
- использование вторичных энергетических ресурсов (ВЭР).
ВЭР подразделяются на горючие (топливные), представляющие химическую энергию отходов технологических процессов переработки топлива и горючих газов металлургии; тепловые ВЭР, представляющие физическую теплоту отходящих газов и жидкостей технологических агрегатов и отходов основного производства, и ВЭР избыточного давления, представляющие потенциальную энергию газов и жидкостей, выходящих из технологических агрегатов, работающих под избыточным давлением.
В зависимости от вида и параметров состояния ВЭР различают четыре направления их использования в производстве:
- топливное направление в виде непосредственного использования горючих компонентов ВЭР в качестве топлива;
- тепловое направление в виде использования тепловых ВЭР;
- силовое направление в виде использования ВЭР для выработки механической или электрической энергии;
- комбинированное направление.
Ниже представлены схемы топливного (рис. 2.3), теплового (рис. 2.4, 2.5, 2.6) и силового (рис. 2.7) направлений использования ВЭР.
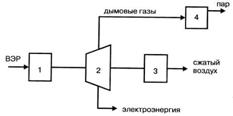
Рисунок 2.3 – Использование горючих ВЭР в качестве топлива в схеме с газовой турбиной:
- 1- топочная камера;
- 2- газовая турбина;
- 3- воздушный компрессор;
- 4- парогенератор
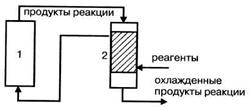
Рисунок 2.4 – Использование тепловых ВЭР
- схеме с теплообменником:
- 1– реактор;
- 2– теплообменник
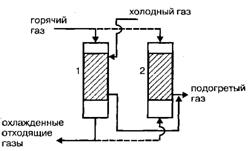
Рисунок 2.5 – Использование тепловых ВЭР в схеме с регенераторами:
- 1– регенераторы, работающие на разогрев камеры;
- 2– регенератор, работающий на подогрев газа
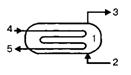
Рисунок 2.6 – Использование тепловых ВЭР для выработки пара в котле-утилизаторе:
- 1- котел-утилизатор;
- 2- подача воды;
- 3- выход пара;
- 4- вход нагретого газа;
- 5- выход охладившего газа
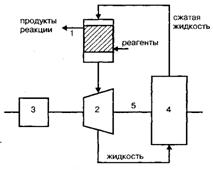
Рисунок 2.7 – Использование части энергии сжатых систем для выработки электроэнергии в схеме «мотор-насос-турбина»:
- 1– реактор;
- 2– жидкостная турбина;
- 3 – мотор;
- 4– насос;
- 5– ось
2.5 Новые виды энергии в химической промышленности
Развитие химической промышленности сопровождается не только количественным ростом энергопотребления, но и качественным изменением его. Это выражается во все более интенсивном внедрении в химическое производство таких новых видов энергии и воздействия на систему как плазмохимическое, ультразвуковое, фото- и радиационное воздействие, действие низковольтного электрического разряда и лазерного излучения. Эти экстремальные воздействия способствуют активации молекул реакционной системы, возникновению в ней возбужденных частиц и инициированию химического, в том числе, с высокой селективностью, процесса. Эта область явлений составляет новую отрасль химии – химию высоких энергий (ХВЭ), изучающую состав, свойства и химические превращения в системах, содержащих возбуждающие частицы.
Среди подобных процессов особо перспективными и универсальными являются плазмохимические процессы, то есть химические превращения, протекающие в плазме. Плазмой называется частично или полностью ионизированный газ, в котором содержатся молекулы, атомы, ионы и электроны:
- A2 ⇔ 2A,
- A → A+ + e.
Различают низкотемпературную плазму с температурой 103-104°К и высокотемпературную с температурой 106-108°К. В химической технологии для получения различных продуктов применяется низкотемпературная плазма, промышленные методы получения которой разработаны. Высокотемпературная плазма используется в установках типа ТОКАМАГ.
В настоящее время исследованы более 70 технологических плазменных процессов, часть которых внедрена в промышленность. К ним относятся:
- синтез эндотермических тугоплавких соединений (карбиды урана и тантала, нитриды титана, алюминия, вольфрама);
- восстановление металлов из их оксидов и солей (железо, алюминий, вольфрам, никель, тантал);
- окисление различных веществ (азот, хлороводород, оксид углерода, метан);
- пиролиз природного газа, нефтепродуктов;
- одностадийный синтез соединений из простых веществ (аммиак, цианистый водород, гидразин, фторуглеводороды);
- синтез соединений, образующихся только в условиях плазмохимического воздействия (озон, дифторид криптона, оксид серы (II), оксид кремния (I)).
В промышленных масштабах плазмохимические процессы применяются для производства ацетилена и водорода из природного газа, ацетилена, этилена и водорода из нефтепродуктов, синтез-газа в производстве винилхлорида, дву-окиси титана и др. Для проведения плазмохимических процессов используются плазменные реакторы различной конструкции.
На рис. 2.8. представлен реактор прямоточного типа, состоящий из четырех основных узлов: плазмотрона, где под воздействием электрической дуги или токов высокой частоты образуется плазма; реактора, в который вводится образовавшаяся плазма и поступают реагенты, закалочного устройства, обеспечивающего быстрое охлаждение (закалку) реакционной смеси и узла улавливания продуктов реакции.
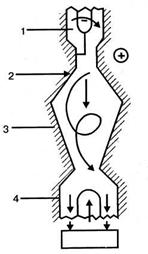
Рисунок 2.8 - Плазменный реактор:
- 1- плазмотрон;
- 2- реактор;
- 3- закалочное устройство;
- 4- узел улавливания
Для плазмохимических реакторов характерно крайне малое время реакции, составляющее от 10-2 до 10-5 секунды. Это определяет весьма малые размеры реактора. Плазмохимические процессы легко управляются, оптимизируются и поддаются моделированию. Затраты энергии на их проведение не превышают затрат энергии на традиционные процессы.
Характерным примером плазмохимического процесса является производство ацетилена пиролизом метана.
- Для реакции 2СН4=С2Н2+3Н2+DН,
- где ΔН=376кДж, константа скорости равна
- Kc= 1012 • [TEX]e^{-79000/RT} [/TEX].
Весьма высокая энергия активации требует высоких температур процесса. Термодинамически реакция становится возможной при температуре выше 1500°К, при которой энергия Гиббса приобретает отрицательное значение:
ΔG = [TEX]96.8-0.064\cdot T[/TEX].
В плазмохимическом процессе получения ацетилена по этой схеме в качестве плазмы используется аргон или водород, а закалка продуктов реакции осуществляется впрыскиванием воды. Степень конверсии метана достигает 0,7, а плазменный реактор диаметром 0,15 м, высотой 0,65 м и объемом 0,05 м3имеет производительность 25000 т ацетилена в год. По энергоемкости плазмохимический метод (14,0 кВт×ч/кг) сопоставим с карбидным методом (15,5кВт×ч/кг), но уступает методам электрокрекинга и термоокислительного пиролиза.