- 7.1 Химическая и принципиальная схемы производства
- 7.2 Окислительный обжиг колчедана
- 7.3 Очистка обжигового (печного) газа
- 7.4 Контактирование оксида серы (IV)
- 7.5 Абсорбция оксида серы (VI)
- 7.6 Технологическая схема производства серной кислоты контактным методом
- 7.7 Товарные сорта серной кислоты
Ключові терміни:
БАВ, СВД, абсорбция оксида серы (VI), абсорбция оксида серы (VI), каталитическое окисление оксида серы (IV), метод двойного двойного контактирования двойной абсорбции (ДКДА), механическая очистка газа, обжиговый (печной) газ, огарок, окисление дисульфида железа, процесс контактирования обжигового газа, специальная очистка газа, электрическая очистка, электрическая очистка газа7.1 Химическая и принципиальная схемы производства
Химическая схема получения серной кислоты из колчедана включает три последовательные стадии:
-
окисление дисульфида железа пиритного концентрата кислородом воздуха:
-
каталитическое окисление оксида серы (IV) избытком кислорода печного газа:
-
абсорбция оксида серы (VI) с образованием серной кислоты:
По технологическому оформлению производство серной кислоты из железного колчедана является наиболее сложным и состоит из нескольких последовательно проводимых стадий.
Принципиальная (структурная) схема этого производства представлена на рис. 7.1.
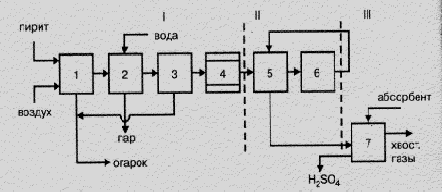
Рисунок 7.1 – Структурная схема производства серной кислоты из флотационного колчедана.
- I – получение обжигового газа: 1 – обжиг колчедана; 2 – охлаждение газа в котле–утилизаторе; 3 – общая очистка газа; 4 – специальная очистка газа;
- II – контактирование: 5 – подогрев газа в теплообменнике; 6 – контактирование;
- III – абсорбция: 7 – абсорбция оксида серы (VI) и образование серной кислоты
7.2 Окислительный обжиг колчедана
Обжиг колчедана в токе воздуха представляет необратимый некаталитический гетерогенный процесс, протекающий с выделением тепла через стадии термической диссоциации дисульфида железа:
и окисления продуктов диссоциации
что описывается общим уравнением:
-
,где DH = –3400 кДж.
Скорость процесса окислительного обжига выражается общим для гетерогенных процессов уравнением
-
(7.1)
- где КМ – коэффициент массопередачи;
- F – поверхность контакта фаз (катализатора);
- DС – движущая сила процесса.
Таким образом, скорость процесса обжига зависит от температуры (через КМ), дисперсности обжигаемого колчедана (через F, концентрации дисульфида железа в колчедане и концентрации кислорода в воздухе (через DС)). На рис. 7.2 представлена зависимость скорости обжига колчедана от температуры и размеров частиц обжигаемого колчедана.
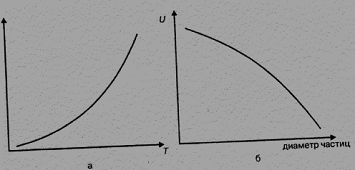
Рисунок 7.2 – Зависимость скорости обжига колчедана от температуры (а) и размеров частиц (б)
Увеличение движущей силы процесса обжига достигается флотацией колчедана, повышающей содержание дисульфида железа в сырье, обогащение воздуха кислородом и применением избытка воздуха при обжиге до 30% сверх стехиометрического количества. На практике обжиг ведут при температуре не выше 10000С, так как за этим пределом начинается спекание частиц обжигаемого сырья, что приводит к уменьшению поверхности их и затрудняет омывание частиц потоком воздуха.
В качестве реакторов для обжига колчедана могут применяться печи различной конструкции: механические, пылевидного обжига, кипящего слоя (КС). Печи кипящего слоя отличаются высокой интенсивностью (до 10000 кг/м2×сут), обеспечивают более полное выгорание дисульфида железа (содержание серы в огарке не превышает 0,005 масс. долей) и контроль температуры, облегчают процесс утилизации теплоты. К недостаткам печей КС следует отнести повышенное содержание пыли в газе обжига, что затрудняет его очистку. В настоящее время печи КС полностью вытеснили печи других типов в производстве серной кислоты из колчедана.
Обжиговый (печной) газ и огарок - продукты окислительного обжига колчедана. Огарок, состоит из оксида железа (III), пустой породы и невыгоревшего остатка дисульфида железа.
Состав обжигового газа зависит от природы сырья, состава и избытка воздуха при его обжиге. В него входят оксид серы (IV), кислород, азот и незначительное количество оксида серы (VI), образовавшегося за счет каталитического действия оксида железа (III). Если не учитывать содержание последнего, то соотношение между кислородом и оксидом серы (IV) в печном газе может быть выражено следующими уравнениями:
- при обжиге колчедана СО2 = 21 – 1,296 СSO2; (7.2а)
- при сжигании серы СО2 = 21 – СSO2; (7.2б)
- при сжигании сероводорода СО2 = 21 – 1,605СSO2, (7.2в)
где СSO2 и СО2 – содержание оксида серы (IV) и кислорода в печном газе.
На практике при обжиге колчедана печной газ содержит 13–14% оксида серы (IV), 2 % кислорода и около 0,1% оксида серы (VI). Так как в печном газе должен быть избыток кислорода для последующего окисления оксида серы (IV), его состав корректируют, разбавляя воздухом до содержания оксида серы (IV) 7–9% и кислорода 11–9%.
7.3 Очистка обжигового (печного) газа
Обжиговый газ необходимо очистить от пыли, сернокислотного тумана и веществ, являющихся каталитическими ядами или представляющих ценность как побочные продукты. В обжиговом газе содержится до 300 г/м3 пыли, которая на стадии контактирования засоряет аппаратуру и снижает активность катализатора, а также туман серной кислоты. Кроме того, при обжиге колчедана одновременно с окислением дисульфида железа окисляются содержащиеся в колчедане сульфиды других металлов. При этом мышьяк и селен образуют газообразные оксиды As2O3 и SeO2, которые переходят в обжиговый газ и становятся каталитическими ядами для ванадиевых контактных масс.
Пыль и сернокислотный туман удаляют из обжигового газа в процессе общей очистки газа, которая включает операции механической (грубой) и электрической (тонкой) очистки. Механическая очистка газа осуществляется пропусканием газа через центробежные пылеуловители (циклоны) и волокнистые фильтры, снижающие содержание пыли в газе до 10–20 г/м3. Электрическая очистка газа в электрофильтрах снижает содержание пыли и тумана в газе до 0,05–0,1 г/м3.
После общей очистки обжиговый газ, полученный из колчедана, обязательно подвергается специальной очистке для удаления остатков пыли и сернокислотного тумана и, главным образом, соединений мышьяка и селена, которые при этом утилизируют. Специальная очистка газа включает операции охлаждения его до температуры ниже температур плавления оксида мышьяка (3150С) и селена (3400С) в башнях, орошаемых последовательно 50% (полая башня) и 20% серной кислотой (башня с насадками), удаления сернокислотного тумана в мокрых электрофильтрах и завершающей осушки газа в скрубберах, орошаемых 95% серной кислотой. Из системы специальной очистки обжиговый газ выходит с температурой 140–1500С.
Оксид селена (IV), извлекаемый из обжигового газа, восстанавливается растворенным в серной кислоте оксидом серы (IV) до металлического селена: который осаждается в отстойниках.
Новым прогрессивным методом очистки обжигового газа является адсорбция содержащихся в нем примесей твердыми поглотителями, например, силикагелем или цеолитами. При подобной сухой очистке обжиговый газ не охлаждается и поступает на контактирование при температуре около 4000С, вследствие чего не требует интенсивного дополнительного подогрева.
7.4 Контактирование оксида серы (IV)
Процесс контактирования обжигового газа – реакция окисления оксида серы IV) до оксида серы (VI), представляет собой гетерогенно–каталитическую, обратимую, экзотермическую реакцию и описывается уравнением
Тепловой эффект реакции зависит от температуры и равен 96,05 кДж при 250С и около 93 кДж при температуре контактирования. Система «SO2 – O2 – SO3» характеризуется состоянием равновесия в ней и скоростью процесса окисления оксида серы (IV), от которых зависит суммарный результат процесса.
7.4.1 Равновесие в системе
Константа равновесия реакции окисления оксида серы (IV) равна
-
(7.3)
где: pSO3 , pSO2, pO2 – равновесные парциальные давления оксида серы (VI), оксида серы (IV) и кислорода соответственно.
Степень превращения оксида серы (IV) в оксид серы (IV) или степень контактирования, достигаемая на катализаторе, зависит от активности катализатора, температуры, давления, состава контактируемого газа и времени контактирования и описывается уравнением
-
, (7.4)
где pSO3 и pSO2 –те же величины, что и в (7.3).
Из уравнений 7.3 и 7.4 следует, что равновесная степень превращения оксида серы (IV) связана с константой равновесия реакции окисления уравнением
-
, (7.5)
где Кр – константа равновесия.
Зависимость Хр от температуры, давления и содержания оксида серы (IV) в обжиговом газе представлена в таблице 7.2 и на рис. 7.3.
Таблица 7.2 – Зависимость Хр от температуры, давления и содержания оксида серы (IV) в обжиговом газе
|
Температура, 0 С* |
Давление, МПа** |
Содержание SO 2 , об.дол. |
||||||
|
1000 |
700 |
400 |
0,1 |
1,0 |
10 |
0,02 |
0,07 |
0,10 |
|
0,050 |
0,436 |
0,992 |
0,992 |
0,997 |
0,999 |
0,971 |
0,958 |
0,923 |
* При давлении 0,1 МПа и содержании оксида серы (IV) 0,07 об. долей.
** При температуре 4000С и содержании оксида серы (IV) 0,07 об.долей.
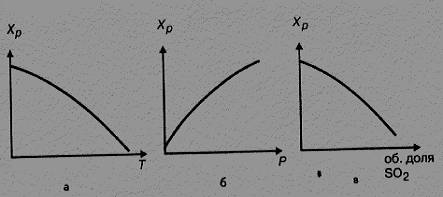
Рисунок 7.3 – Зависимость равновесной степени превращения оксида серы (IV) в оксид серы (VI) от температуры (а), давления (б) и содержания оксида серы (IV) в газе (в)
Из уравнения 7.5 и табл. 7.2 следует, что с понижением температуры и повышением давления контактируемого газа равновесная степень превращения Хр возрастает, что согласуется с принципом Ле–Шателье. В то же время при постоянных температуре и давлении равновесная степень превращения тем больше, чем меньше содержание оксида серы (IV) в газе, то есть чем меньше отношение SO2 : O2. Это отношение зависит от вида обжигаемого сырья и избытка воздуха. На этой зависимости основана операция корректирования состава печного газа, то есть разбавление его воздухом для снижения содержания оксида серы (IV).
Степень окисления оксида серы (IV) возрастает с увеличением времени контактирования, приближаясь к равновесию по затухающей кривой (рис. 1.4). Следовательно, время контактирования должно быть таким, чтобы обеспечить достижение равновесия в системе. Из рис. 1.4 следует, что чем выше температура, тем скорее достигается равновесие (t1 < t2), но тем меньше равновесная степень превращения ( Х1 < X2 при Т1 > T2). Таким образом, выход оксида серы (VI) зависит как от температуры, так и от времени контактирования. При этом для каждого времени контактирования зависимость выхода от температуры выражается соответствующей кривой, имеющей максимум. Очевидно, что огибающая эти максимумы линия АА (рис.1.5) представляет кривую оптимальных температур для различного времени контактирования, близкую к равновесной кривой.
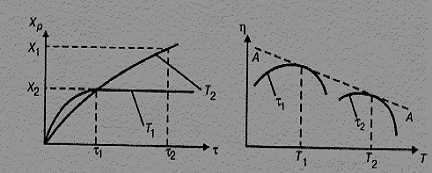 |
|
|
Рисунок 7.4 – Зависимость Хр от времени контактирования |
Рисунок 7.5 – Зависимость выхода оксида серы (VI) от температуры при различном времени контактирования |
7.4.2 Скорость окисления оксида серы (IV)
От скорости окисления зависит количество оксида серы (IV), окисляющееся в единицу времени и, следовательно, объем контактной массы, размеры реактора и другие характеристики процесса. Организация этой стадии производства должна обеспечить возможно более высокую скорость окисления при максимальной степени контактирования, достигаемой в данных условиях.
Энергия активации реакции окисления оксида серы (IV) кислородом в оксид серы (VI) весьма велика. Поэтому при отсутствии катализатора реакция окисления даже при высокой температуре практически не идет. Применение катализатора позволяет снизить энергию активации реакции и увеличить скорость окисления в соответствии с зависимостью для константы скорости:
-
, (7.6)
- где k0 – константа скорости химической реакции;
- E – энергия активации, Дж/моль;
- R – универсальная газовая постоянная (8,326 Дж/моль * К);
- T – температура, 0К.
Если без катализатора реакция окисления 2SO2 + O2 = 2 SO3 протекает как реакция третьего порядка с энергией активации более 280 кДж/моль, то в присутствии ванадиевого катализатора ее порядок снижается до 1,8, а энергия активации составляет 92 кДж/моль.
В производстве серной кислоты в качестве катализатора применяют константные массы на основе оксида ванадия (V) марок БАВ и СВД, названные так по начальным буквам элементов, входящих в их состав:
БАВ (барий, алюминий, ванадий) состава:
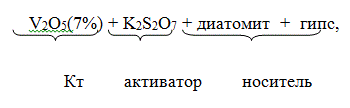
СВД (сульфо-ванадато-диатомовый) состава:
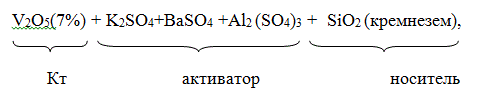
Предполагается, что процесс окисления оксида серы (IV) на этих катализаторах идет через стадию диффузии реагентов к поверхности катализатора, на которой образован комплекс оксида ванадия (V) с активатором, сорбции реагентов на катализаторе с последней десорбцией продукта реакции (оксида серы (VI)):
Схема действия ванадиевого катализатора представлена на рис. 1.6.
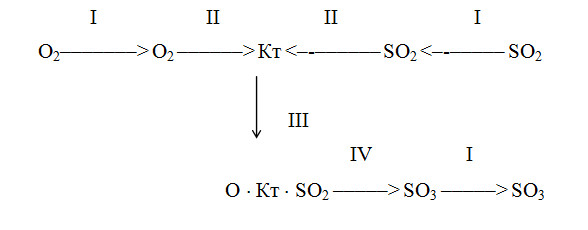
Рисунок 7.6 – Схема действия катализатора: I – диффузия; II – сорбция; III – образование комплекса; IV – десорбция
Процесс катализа состоит из нескольких последовательно протекающих элементарных актов: диффузии молекул азота, кислорода и оксида серы (IV) к катализатору (I), хемосорбции молекул реагентов на поверхности катализатора (II), химического взаимодействия кислорода и оксида серы (IV) на поверхности катализатора с переносом электронов от молекул оксида серы к молекулам кислорода и образованием неустойчивых комплексов (III) , десорбции образовавшихся молекул оксида серы (VI) (IV) и диффузии их из пор и с поверхности катализатора в газовую фазу.
Температура зажигания контактных ванадиевых масс составляет 380–4200С и зависит от состава контактируемого газа, повышаясь с уменьшением содержания в нем кислорода. Контактные массы должны находиться в таком состоянии, чтобы были обеспечены минимальное гидравлическое сопротивление потоку газа и возможность диффузии компонентов через слой катализатора. Для этого контактные массы для реакторов с неподвижным слоем катализатора формуются в виде гранул, таблеток или колец средним диаметром около 5 мм, а для реакторов кипящего слоя в виде шариков диаметром около 1 мм.
Для описания скорости окисления оксида серы (IV) в оксид серы (VI) на ванадиевом катализаторе при неподвижном слое катализатора предложены различные кинетические уравнения. К ним относятся уравнение 1.7, связывающее скорость реакции со степенью превращения оксида серы (IV) , константой скорости реакции, константой равновесия и давлением газа:
-
, (7.7)
-
, (7.8)
- где Х – равновесная степень превращения оксида серы (IV);
- k – константа скорости реакции окисления;
- а – начальная концентрация оксида серы (IV) в газе;
- b – начальная концентрация кислорода в газе;
- Р – общее давление газа;
- Кр – константа равновесия реакции .
Из уравнений 7.7 и 7.8 следует, что скорость окисления зависит от константы скорости реакции, сильно возрастающей при повышении температуры (уравнение 1.6). Однако при этом уменьшается константа равновесия Кр (уравнение 1.3) и уменьшается значение члена в уравнении 1.7. Таким образом, скорость процесса окисления оксида серы (IV) зависит от двух величин, изменяющихся с ростом температуры в противоположном направлении. Вследствие этого кривая зависимости скорости окисления от температуры должна проходить через максимум. Из уравнения 1.7 также следует, что скорость окисления оксида серы (IV) тем больше, чем меньше достигаемая в этом процессе степень превращения оксида серы (IV) в оксид серы (VI). Вследствие этого для каждой степени превращения зависимость скорости реакции от температуры будет выражаться индивидуальной кривой, имеющей максимум. На рис. 7.7 представлена серия подобных кривых, соответствующих различным степеням превращения для газа постоянного состава. Из него следует, что скорость реакции окисления достигает максимума при определенных значениях температур, которые тем выше, чем меньше эта степень превращения. Линия АА, соединяющая точки оптимальных температур, называется линией оптимальной температурной последовательности (ЛОТ) и указывает, что для достижения наилучших результатов процесс контактирования следует начинать при высокой температуре, обеспечивающей большую скорость процесса (на практике около 6000С), а затем для достижения высокой степени превращения снижать температуру, выдерживая температурный режим по ЛОТ.
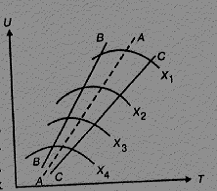
Рисунок 7.7 – Зависимость скорости окисления оксида серы (IV) от температуры при различных степенях превращения Х1
Линии ВВ и СС на рис. 1.7 очерчивают область допустимых колебаний температуры в реальном технологическом процессе контактирования.
Обеспечение высокой температуры в начале процесса окисления требует больших затрат энергии на подогрев газа, поступающего на контактирование. Поэтому на практике температуру газа на входе в контактный аппарат, поступающего на первый слой катализатора, задают лишь несколько выше температуры зажигания (порядка 4200С). В ходе реакции выделяется большое количество тепла, и так как процесс в слое катализатора идет без отвода тепла, то температура газа повышается по адиабате 1, пока не достигает величины, равной 0,8 ЛОТ (рис.7.8). После этого газ охлаждают в теплообменнике (линия а) до тех пор, пока температура не достигнет величины 0,8 ЛОТ. После теплообменника газ направляют на второй слой катализатора и ведут процесс по адиабате 2, затем снова охлаждают и продолжают процесс до тех пор, пока не будет достигнута заданная степень контактирования Х. Обычно для этого достаточно иметь в контактном аппарате 4–5 слоев контактной массы. В табл. 7.3 представлен температурный режим 4–слойного контактного аппарата с промежуточным теплообменом, установленный в соответствии с изложенным выше принципом.
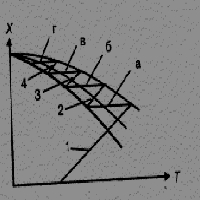
Рисунок 7.8 – Диаграмма контактирования для 4 слоев Кт: 1,2,3,4 – адиабаты; а, б, в, г – линии охлаждения
Таблица 7.3 – Температурный режим контактного узла
|
Слой |
I |
II |
III |
IV |
|
Температурный режим в контакт–ном аппарате, 0 С |
440–600 |
460–500 |
440–450 |
420–425 |
|
Температурный режим в теплооб– меннике, 0 С |
600–460 |
500–440 |
450–420 |
420 |
|
Х р |
0,70 |
0,90 |
0,96 |
0,98 |
Таким образом, противоречие между кинетикой и термодинамикой процесса окисления оксида серы (IV) достаточно успешно снимается конструкцией и температурным режимом работы контактного аппарата. Это достигается разбивкой процесса на стадии, каждая из которых отвечает оптимальным условиям протекания процесса контактирования. Тем самым определяются и начальные параметры режима контактирования: температура 400–4400С, давление 0,1 Мпа, содержание оксида серы (IV) в газе 0,07-0,09 об. Долей, содержание кислорода в газе 0,09- 0,11 об. долей.
Реакторы или контактные аппараты для каталитического окисления оксида серы (IV) по своей конструкции делятся на аппараты с неподвижным слоем катализатора (полочные или фильтрующие), в которых контактная масса расположена в 4–5 слоях, и аппараты кипящего слоя. Отвод тепла после прохождения газом каждого слоя катализатора осуществляется путем введения в аппарат холодного газа или воздуха или с помощью встроенных в аппарат или вынесенных отдельно теплообменников (принцип рекуперации).
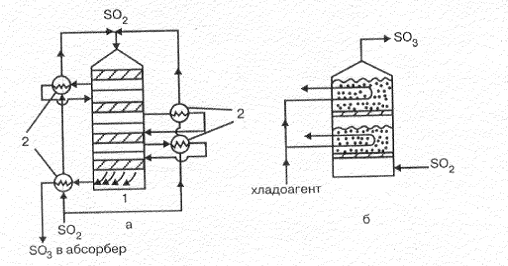
Рисунок 7.9 – Конструкции контактных аппаратов: а – контактный узел: 1 – контактный аппарат, б – контактный аппарат кипящего слоя; 2 - теплообменник.
Совокупность контактного аппарата, теплообменников и газопроводов представляет контактный узел. На рис. 7.9 представлены контактный узел, состоящий из контактного аппарата фильтрующего типа, и выносных теплообменников, и контактный аппарат кипящего слоя.
К преимуществам контактных аппаратов кипящего слоя относятся:
- высокий коэффициент теплоотдачи от катализатора в состоянии кипящего слоя к поверхности теплообменника (в 10 раз больше, чем от газа), что позволяет без перегрева вести контактирование печного газа с высоким содержанием оксида серы (IV) и снизить температуру зажигания катализатора;
- нечувствительность к пыли, вносимой вместе с печным газом.
7.4.3 Двойное контактирование
Важнейшей задачей совершенствования сернокислотного производства являются увеличение степени контактирования и снижение выбросов оксида серы (IV) в атмосферу. В обычном процессе повышение степени контактирования выше 0,98 дол. Единицы нецелесообразно, так как связано с резким увеличением количества и числа слоев контактной массы. Однако даже при этой максимальной для обычного процесса степени контактирования выброс оксида серы (IV) может достигать на современных установках 35–60 т/сутки. Помимо значительных потерь продукции это вызывает необходимость в сложных и дорогостоящих очистных сооружениях для нейтрализации отходящих газов.
Метод двойного двойного контактирования двойной абсорбции (ДКДА) применяют для увеличения конечной степени контактирования и ведут процесс окисления оксида серы (IV) в две стадии. На первой стадии контактирование ведут до степени превращения, не превышающей 0,90–0,92 дол. , после чего из контактированного газа выделяют оксид серы (VI). Затем проводят вторую стадию контактирования до степени превращения оставшегося в газе оксида серы (IV) 0,95 дол. единицы. Конечная степень контактирования определяется в этом случае как
-
, (7.9)
- где Х1 – степень контактирования на первой стадии;
- Х2 – степень контактирования на второй стадии.
Метод двойного контактирования позволяет повысить степень контактирования до 0,995 дол. ед. и на несколько порядков снизить выброс оксида серы (IV) в атмосферу. На рис. 7.10 представлена схема двойного контактирования с использованием контактного аппарата фильтрующего типа, применяемая в установках ДК–ДА.
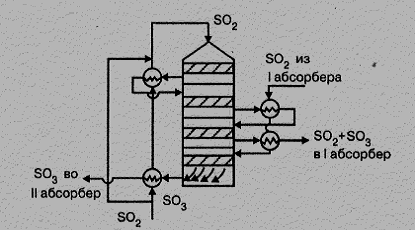
Рисунок 7.10 – Схема двойного контактирования
7.5 Абсорбция оксида серы (VI)
Абсорбция оксида серы (VI) является последней стадией в производстве серной кислоты контактным способом из контактированного газа и превращение его в серную кислоту или олеум. Абсорбция оксида серы (VI) представляет обратимую экзотермическую реакцию и описывается уравнением
Тепловой эффект реакции зависит от значения n и для n = 1 (образование моногидрата серной кислоты) равен 92 кДж.
В зависимости от количественного соотношения оксида серы (VI) и воды может быть получен продукт различной концентрации:
- при n > 1 олеум;
- при n = 1 моногидрат (100% серная кислота);
- при n < 1 водный раствор кислоты (разбавленная серная кислота).
Для процесса абсорбции оксида серы (VI) существенное значение имеет природа абсорбента. Скорость абсорбции описывается уравнением
-
, (7.10)
- где К – коэффициент абсорбции;
- F – поверхность раздела фаз «абсорбент–газ»;
- Dр – движущая сила процесса абсорбции.
Движущая сила процесса абсорбции
-
где p SO3 – парциальное давление оксида серы (VI) в газе; p*SO3 – равновесное давление оксида серы (VI) над сорбентом.
Так как p*SO3 задается составом газа, то движущая сила и, следовательно, скорость процесса абсорбции будут тем больше, чем меньше равновесное давление оксида серы (VI) над сорбентом.
Кроме этого, при высоком равновесном давлении над сорбентом паров воды p*Н2О вследствие взаимодействия молекул воды с молекулами оксида серы (VI) образуются пары серной кислоты, конденсирующиеся с возникновением трудно улавливаемого тумана серной кислоты:
Таким образом, наилучшей поглощающей способностью будет обладать абсорбент с минимальным равновесным давлением над ним оксида серы (VI) и паров воды. Этому условию в максимальной степени удовлетворяет азеотроп серной кислоты концентрацией 98,3%. Использование серной кислоты более низкой концентрации приводит к интенсивному образованию тумана, а применение 100% кислоты или олеума – к снижению степени абсорбции. На рис. 7.11 представлена зависимость скорости абсорбции оксида серы (VI) от концентрации серной кислоты, используемой в качестве абсорбента.
Абсорбция оксида серы (VI) сопровождается выделением значительного количества тепла. Поэтому для обеспечения полноты поглощения оксида серы (VI) процесс ведут при охлаждении газа и абсорбента до 800С и используют аппараты с большим абсорбционным объёмом.
На рис. 7.11 представлена схема абсорбции.
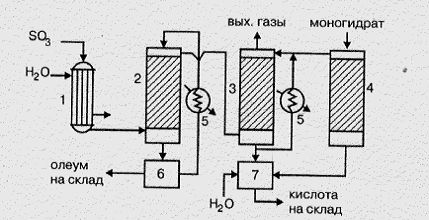
Рисунок 7.11 – Схема двухстадийного процесса абсорбции:
- холодильник газа;
- олеумный абсорбер;
- моногидратный абсорбер;
- сушильная башня;
- холодильник жидкого продукта;
- сборник олеума;
- сборник моногидрата
Подобная схема абсорбции позволяет получать, кроме контактной серной кислоты концентрацией 92–93%, также олеум различной концентрации.
7.6 Технологическая схема производства серной кислоты контактным методом
В настоящее время в производстве серной кислоты и олеума контактным методом наиболее распространенной является технологическая схема с использованием принципа двойного контактирования «ДК–ДА» (двойное контактирование – двойная абсорбция). Часть подобной схемы, за исключением печного отделения и отделения общей очистки печного газа, технологически однотипных для всех схем, представлена на рис. 7.12
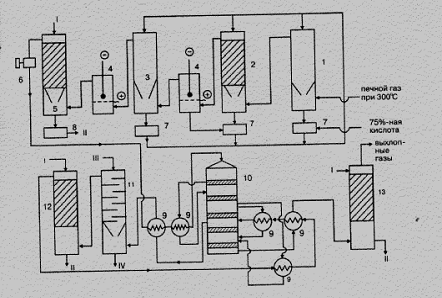
Рисунок 7.12 – Технологическая схема производства серной кислоты из колчедана двойным контактированием ДК–ДА
- полая промывная башня;
- промывная башня с насадкой;
- увлажнительная башня;
- электрофильтры;
- сушильная башня;
- турбогазодувка;
- сборник 75% кислоты;
- сборник продукционной кислоты;
- теплообменники;
- контактный аппарат;
- олеумный абсорбер;
- моногидратныq абсорбер.
- моногидратныq абсорбер.
Потоки продуктов:- I – охлажденная 98% кислота;
- II – продукционная кислота на охлаждение;
- III – охлажденный олеум или моногидрат;
- IV – продукционный олеум на охлаждение.
Производительность установки до 1500 т/сут. по моногидрату. Расходные коэффициенты (на 1 т моногидрата): колчедан 0,82 т, вода 50 м3, электроэнергия 82 кВт*ч.
7.7 Товарные сорта серной кислоты
Современная промышленность выпускает несколько сортов серной кислоты и олеума, различающихся концентрацией и чистотой (табл.7.4). Чтобы уменьшить возможность кристаллизации продуктов при перевозке и хранении, а также в самом производстве, установлены стандарты на товарные сорта, концентрации которых отвечают эвтектическим составам с наиболее низкими температурами кристаллизации.
При определении технико–экономических показателей сернокислотного производства расчеты производимой продукции ведутся, обычно, на 100% серную кислоту (моногидрат). Для пересчета массы олеума на массу моногидрата используется формула
-
, (1.11)
где- mм – масса моногидрата;
- mол – масса олеума;
- mSO3 – массовая доля свободного оксида серы (VI) в олеуме.
Таблица 7.4 – Товарные сорта серной кислоты и олеума
|
Сорт продукта |
Содержание H2SO4, % |
Содержание своб. SO3, % |
Температура кристаллиза–ции, 0С |
|
Башенная кислота |
75,0 |
0,0 |
–29,5 |
|
Контактная кислота |
92,5 |
0,0 |
–22,0 |
|
Олеум |
104,5 |
20,0 |
+2,0 |
|
Высокопроцентный олеум |
114,6 |
65,0 |
–0,35 |
Пример решения задачи
Составить материальный баланс сушильного отделения обжигового газа. Объём обжигового газа V м3. Состав обжигового газа (% об): SO2 – a, O2 – b, N2 – 79. Водяных паров в газе 138 м3 или 110,9 кг. Газ разбавляется воздухом до 7,5% об. SO2. Водяные пары поглощаются серной кислотой с массовой долей ω1 = 94%. Кислота разбавляется до массовой доли ω2 = 93,5%. Уходящий из сушильного отделения газ содержит 0,2 г/м3 водяных паров. МSO2 = 64 г/моль, МО2 = 32 г/моль, МN2 =28 г/моль.
Исходные данные
V обж.газа= 1000 м3; а – 9,6 % (об.) b – 11,4 % (об.)
Решение
Рассчитаем состав сухого обжигового газа:
VSO2 = a∙ V обж.газа/100 = 9.6 ∙1000/100 = 276,38 м3, или mSO2 = VSO2∙ МSO2/22.4 =789,66м3.
Аналогичным образом рассчитывают объём и массу кислорода и азота, входящих в состав обжигового газа, и данные заносят в таблицу:
Объем сухого газа после разбавления его воздухом
Объем сухого воздуха, который нужно добавить к газу
![]()
Принимаем относительную влажность воздуха равной 50% (0,5 долей единицы) и температуру воздуха 23◦С. Этой температуре соответствует давление насыщенного водяного пара Р=2786,4 Па (20,9 мм рт.ст.)
Объем влаги, вносимой воздухом:
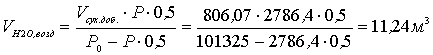
Состав воздуха, добавленного к газу
|
м3 |
кг |
|||
|
O2 |
806,07∙0,21 |
= |
169,27 |
241,82 |
|
N2 |
806,07∙0,79 |
= |
636,80 |
796,00 |
|
H2O |
11,24 |
9,03 |
Общая масса влаги, вносимая газом и воздухом mH2O,общ. = 110,90 + 9,03 = 119,03 кг
Масса влаги в газе, уходящем из сушильного отделения
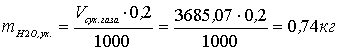
Масса влаги, поглощаемой кислотой
mH2O,погл. = mH2O,общ. – mH2O,ух.= 119,93 – 0,74 = 119,19 кг
Массу кислоты х, необходимой для осушки газа, вычисляем по уравнению баланса моногидрата в поступающей и уходящей кислоте:
х • ω1 H2SO4 = (х + mH2Oпогл.) = ω2 H2SO4
0,94х = (х+119,19) • 0,935
0,94х – 0,935х = 111,44
х = 22288 кг
Объем кислоты (S = 1800 кг/м3)
![]()
Исходя из практических данных принимаем, что 0,3% (об.) SO2 извлекается из газа, растворяясь в H2SO4. Масса растворившегося в кислоте оксида серы (IV) SO2 составляет
mSO2,раств. = VSO2 • 0,003 = 276,38 • 0.003 = 0,83 м3 или 2,37 кг
Выходящий из сушильного отделения газ содержит
|
м3 |
кг |
|
|
SO2 |
276,38 – 0,83 = 275,55 |
787,3 |
|
N2 |
2274,1 + 636,8 = 2911,21 |
3639,01 |
|
O2 |
328,21 + 169,27 = 497,48 |
710,69 |
|
H2O |
– |
0,74 |
Масса выходящей из сушильного отделения кислоты
mH2SO4 вых. = х + mH2O погл.+ mSO2 раств. = 22288 + 119,19 + 2,37 = 22409,56
Массовая доля H2SO4 в этой кислоте
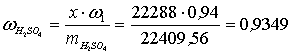
или 93,49%
Материальный баланс процесса осушки обжигового газа
|
Приход |
||||
|
кг |
м3 |
|||
|
газ |
SO2 |
789,66 |
276,38 |
|
|
N2 |
2843,01 |
2274,41 |
||
|
O2 |
468,87 |
328,21 |
||
|
H2O |
110,90 |
138,00 |
||
|
воздух |
N2 |
796,00 |
636,80 |
|
|
O2 |
241,82 |
169,27 |
||
|
H2O |
9,03 |
11,24 |
||
|
H2SO4 (94%) |
22288 |
|||
|
Всего |
27547,29 |
|||
|
Расход |
||||
|
газ |
SO2 |
787,30 |
275,55 |
|
|
N2 |
3639,01 |
2911,21 |
||
|
O2 |
710,69 |
497,48 |
||
|
H2O |
0,74 |
|||
|
H2SO4 (93,49%) |
22409,56 |
|||
|
Всего |
27547,30 |
|||



